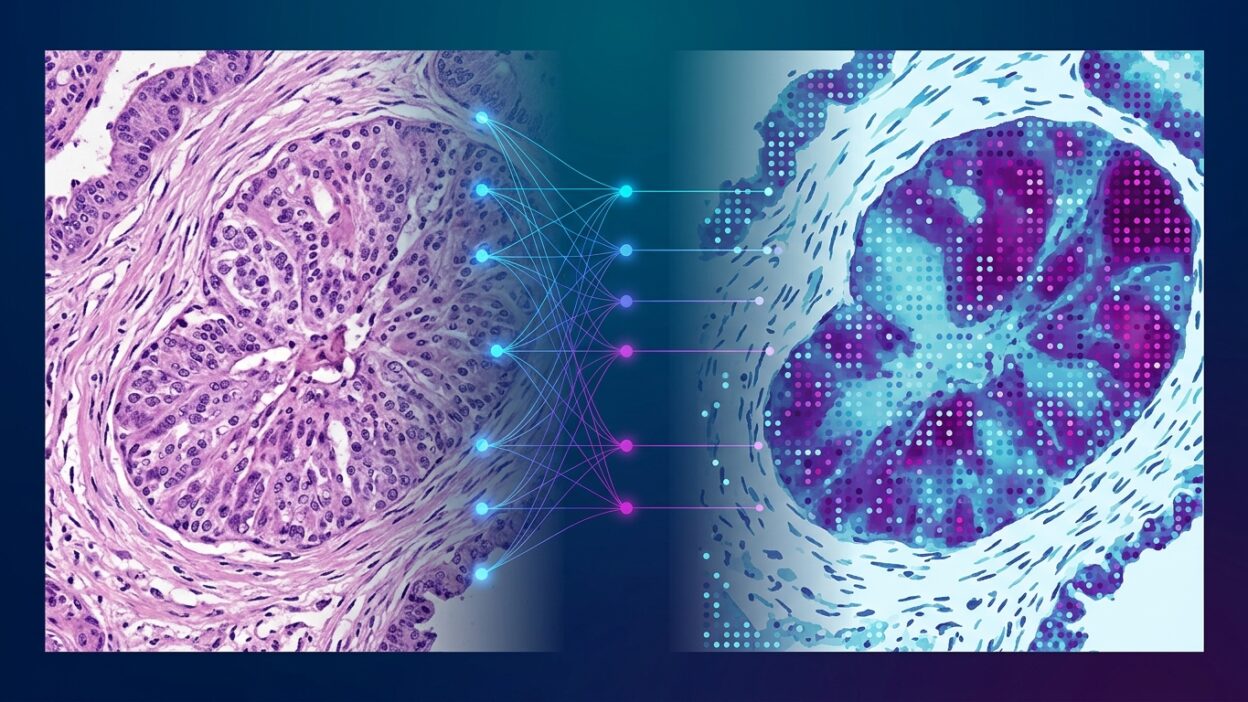
نشرت مجلة Cell دراسة بعنوان AI-predicted spatial transcriptomics unlocks breast cancer biomarkers from pathology تقترح مساراً عملياً لتوسيع استخدام البيانات المكانية في سرطان الثدي من دون إجراء spatial transcriptomics لكل عينة. الفكرة المباشرة: نموذج عميق باسم Path2Space يتعلم من شرائح الهستوباثولوجي المقترنة ببيانات ST، ثم يتنبأ بالتعبير الجيني المكاني مباشرة من الصورة.
هذا النوع من العمل يهم الباثولوجي الرقمي لأنه لا يتعامل مع الشريحة كصورة تصنيفية فقط. الهدف هنا ليس التنبؤ بدرجة الورم أو subtype جاهز، بل بناء طبقة جزيئية مكانية متوقعة فوق النسيج، بحيث تصبح بنية الورم والـ TME قابلة للتحليل على مستوى أفواج كبيرة لا يمكن عملياً فحصها كلها بتقنيات ST عالية الكلفة.
الفرق عن كثير من نماذج WSI السابقة أن المخرج ليس label واحداً على مستوى الشريحة أو tile. المخرج خريطة تعبير، أي أن السؤال ينتقل من “ماذا يوجد في العينة؟” إلى “أين تظهر الإشارة الجزيئية داخل العينة؟”. هذه النقلة تجعل النموذج أقرب إلى لغة الباثولوجي، لأن التفسير في الشريحة يبدأ دائماً من المكان والعلاقة بين المكونات.
ما الذي فعله الباحثون؟
قدّم Shulman وزملاؤه نموذج Path2Space للتنبؤ بالتعبير المكاني لآلاف الجينات من شرائح سرطان الثدي. بحسب ملخص الدراسة، تدرّب النموذج على مجموعة واسعة من بيانات spatial transcriptomics الخاصة بسرطان الثدي، ثم قورن مع 21 طريقة منشورة. تفوق النموذج في مهمة التنبؤ بالتعبير الجيني المكاني، ثم استُخدم لرسم خرائط tumor microenvironment في 976 ورماً من TCGA.
الخطوة المهمة ليست المقارنة العددية فقط. استخدام النموذج على TCGA يعني تحويل أرشيف غني بالمتابعة السريرية والبيانات الجزيئية إلى مساحة يمكن فيها اختبار فرضيات مكانية لم تكن متاحة سابقاً على هذا الحجم. في العادة نملك H&E وبيانات bulk omics، لكننا نفتقد التنظيم المكاني للنسخ الجيني داخل الورم وحوله. Path2Space يحاول ملء هذه الفجوة بتنبؤ محسوب من الصورة.
من الصورة إلى خريطة TME قابلة للقياس
تذكر الدراسة أن النموذج استنتج وفرة أنواع خلوية داخل TME بدقة، وحدد ثلاث مجموعات مكانية في سرطان الثدي ارتبطت بفروق في البقاء. هذه نقطة حساسة للباثولوجيين: التقسيم هنا ليس مبنياً على مظهر مورفولوجي منفصل عن البيولوجيا، ولا على bulk RNA يلغي المكان. إنه تقسيم يحاول ربط النمط النسيجي بالتعبير الجيني وبالتوزيع المكاني للخلايا.
إذا ثبتت هذه النتائج في أفواج خارجية وبروتوكولات تصوير مختلفة، فقد يصبح لدينا إطار جديد لاستخراج biomarkers من الشرائح المؤرشفة. ليس بديلاً مباشراً عن HER2 IHC أو ISH أو اختبارات النسخ الجيني المعتمدة، بل طبقة إضافية قد تكشف علاقات مكانية لا تظهر في القياسات المتوسطة للعينة.
الاستجابة للعلاج: أين تصبح الخريطة مفيدة؟
أحد أقوى ادعاءات الورقة أن الخرائط المكانية منخفضة الكلفة، والمستخرجة من H&E عبر Path2Space، حسّنت توقع الاستجابة للعلاج الكيماوي و trastuzumab مقارنة بواسمات تقليدية مبنية على bulk sequencing. هذا الادعاء يحتاج قراءة نقدية عند صدور النص الكامل والبيانات التفصيلية، لكنه يضع سؤالاً مهماً أمام المجال: هل المكان نفسه biomarker؟
في سرطان الثدي، مكان الخلايا المناعية، مناطق hypoxia، تماس الخلايا الورمية مع stroma، وتغاير التعبير داخل الكتلة قد تكون أهم من المتوسط العام لبعض الجينات. الباثولوجي يرى هذه العلاقات يومياً، لكن تحويلها إلى متغيرات كمية متصلة بالاستجابة العلاجية ظل صعباً. نماذج مثل Path2Space تحاول ترجمة هذا الحس البصري إلى خرائط جينية مكانية قابلة للاختبار.
ما الذي لا يجب أن نستنتجه بسرعة؟
لا تعني الدراسة أن ST أصبح غير ضروري. النموذج يتعلم من ST، ويتأثر بجودة التدريب، ونوع المنصة، وتحضير النسيج، والماسح، والتلوين، وتوزيع الحالات. كما أن التنبؤ بالتعبير الجيني من الصورة يبقى تنبؤاً احتماليّاً، لا قياساً مباشراً. أي استخدام سريري سيحتاج تحققاً مستقلاً، ومعايير أداء واضحة، وتحليلاً لفشل النموذج في الحالات النادرة أو المعالجة أو ذات النخر الشديد.
هناك أيضاً سؤال قابلية النقل. نموذج مدرب على سرطان الثدي قد لا ينقل نفس الجودة إلى أورام أخرى من دون بيانات تدريب مناسبة. وحتى داخل سرطان الثدي، اختلاف subtypes والعلاجات السابقة وجودة الشرائح قد يغيّر الإشارة. لذلك تبدو القيمة الأقرب حالياً في البحث الترجمي وبناء الفرضيات على أرشيفات كبيرة، أكثر من كونها أداة قرار سريري جاهزة.
لماذا يهم هذا للباثولوجي الرقمي؟
القيمة العملية في Path2Space أنه يعيد تعريف ما يمكن استخراجه من H&E. الشريحة ليست مجرد مدخل لنموذج تصنيف، بل قد تصبح مدخلاً لبناء طبقة spatial omics تقريبية فوق آلاف الحالات المؤرشفة. هذا يفتح باباً لتجارب biomarker discovery على نطاق كان مكلفاً جداً إذا اعتمد بالكامل على ST.
بالنسبة للباثولوجيين، الاتجاه واضح: النماذج المقبلة لن تكتفي بقول “سرطان” أو “ليس سرطاناً”. ستقترب من وصف بيولوجيا الورم مكانياً، وتربط البنية النسيجية بالنسخ الجيني، وبالاستجابة العلاجية، وبالنتائج السريرية. السؤال المهني لن يكون هل تحل الخوارزمية محل قراءة الشريحة، بل كيف نراجع خرائطها، ونختبر حدودها، ونقرر متى تضيف معلومة حقيقية فوق ما نعرفه من morphology و IHC و molecular testing.
الخلاصة
Path2Space يقدم مثالاً ناضجاً على اتجاه مهم في الباثولوجي الرقمي: تحويل الشرائح الروتينية إلى خرائط جزيئية مكانية متوقعة. الورقة لا تغلق ملف spatial transcriptomics، لكنها تقترح طريقة لاستخدام ST كبيانات تدريب ثم تعميم بعض إشاراتها على أفواج H&E كبيرة. إذا صمدت النتائج في التحقق الخارجي، فقد تصبح هذه المقاربة أداة قوية لاكتشاف biomarkers علاجية في سرطان الثدي، وربما في أورام أخرى لاحقاً.
المصدر: Shulman ED وآخرون. Cell. 2026. DOI: 10.1016/j.cell.2026.04.023.